पाठ के दिए गए प्रश्नोत्तर
प्रश्न 1.
निम्नलिखित के लिए मोलर द्रव्यमान का परिकलन कीजिए-
(i) H20
(ii) CO2
(iii) CH4
उत्तर
(i) H20 का मोलर द्रव्यमान = (2×1.008) + (1600) = 18.016 amu
(ii) CO2 का मोलर द्रव्यमान = 12.01+ (2×1600)= 44.01 amu
(iii) CH4, का मोलर द्रव्यमाने = 12.01+ (4×1.008)= 16.042 amu
प्रश्न 2.
सोडियम सल्फेट (Na2SO4) में उपस्थित विभिन्न तत्वों के द्रव्यमान प्रतिशत का परिकलन कीजिए।
उत्तर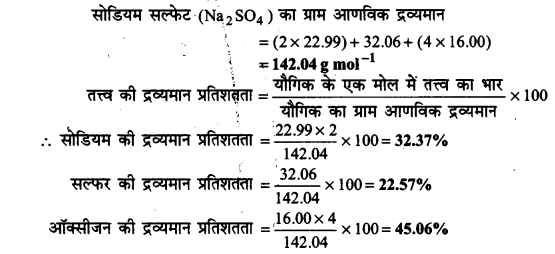
Class 11th रसायन विज्ञान की कुछ मूल अवधारणाएँ Solution - RDS TEAM
प्रश्न 3.
आयरन के उस ऑक्साइड का मूलनुपाती सूत्र ज्ञात कीजिए जिसमें द्रव्यमान द्वारा 69.9% आयरन और 30.1% ऑक्सीजन है।
उत्तर
>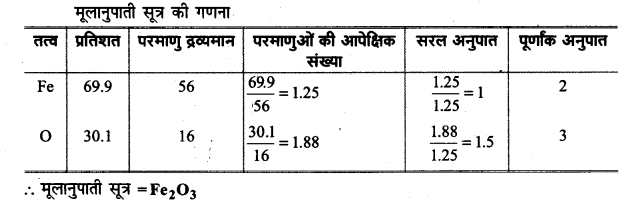
∴ मूलानुपाती सूत्रे =Fe203
प्रश्न 4.
प्राप्त कार्बन डाइऑक्साइड की मात्रा का परिकलन कीजिए। जब-
(i) 1 मोल कार्बन को हवा में जलाया जाता है और
(ii) 1 मोल कार्बन को 16 g ऑक्सीजन में जलाया जाता है।
उत्तर
ऑक्सीजन/वायु में कार्बन निम्न प्रकार से जलता ह-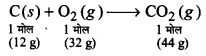
(i) हवा में ऑक्सीजन की प्रचुर मात्रा है। इस कारण से ज्वलन पूर्ण होता है। अतः 1 मोल कार्बन | के दहन से उत्पन्न CO2 = 44 g
(ii) इस स्थिति में ऑक्सीजन एक सीमांत अभिकर्मक है। केवल 0.5 मोल कार्बन के जलेंगे।
∴ 32 g ऑक्सीजन से उत्पन्न CO2 = 44g
∴ 16 g ऑक्सीजन से उत्पन्न CO2= [latex]\frac { 44 }{ 32 } \times 16[/latex]= 22 g
Class 11th रसायन विज्ञान की कुछ मूल अवधारणाएँ Solution - RDS TEAM
प्रश्न 5.
सोडियम ऐसीटेट (CH3COONa) का 500 mL, 0.375 मोलर जलीय विलयन बनाने के लिए उसके कितने द्रव्यमान की आवश्यकता होगी? सोडियम ऐसीटेट का मोलर द्रव्यमान 82.0245 g mol-1 है।
उत्तर
जलीय विलयन की मोलरता निम्न समीकरण से व्यक्त की जा सकती है-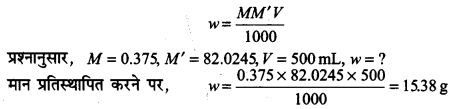
अत: सोडियम ऐसीटेट के द्रव्यमान की आवश्यक मात्रा = 15.38 g
प्रश्न 6.
सान्द्र नाइट्रिक अम्ल के उस प्रतिदर्श का मोल प्रति लीटर में सान्द्रता का परिकलन कीजिए जिसमें उसका द्रव्यमान प्रतिशत 69% हो और जिसका घनत्व 1.41 g mL-1 हो।।
उत्तर
दिया गया प्रतिदर्श 69% है अर्थात् 100 g विलयन में केवल 69 g नाइट्रिक अम्ल है। नाइट्रिक अम्ल का मोलर द्रव्यमान =1+14+ (3×16) = 63g mol-1
∴ 69 g शुद्ध नाइट्रिक अम्ल (जो विलयन के 100 g में उपस्थित है) में उपस्थित मोलों की संख्या = [latex]\frac { 69 }{ 63 } =1.095[/latex]
Class 11th रसायन विज्ञान की कुछ मूल अवधारणाएँ Solution - RDS TEAM
प्रश्न 7.
100 g कॉपर सल्फेट (CuSO4) से कितना कॉपर प्राप्त किया जा सकता है?
उत्तर
CuSO4 का मोलर द्रव्यमान = 63.5 + 32+ (4×16)= 1595 g mol-1
1 मोल (159.5 g) CuSO4 में Cu का 1 ग्राम परमाणु (63.5 g) उपस्थित रहता है
∴ 100 g कॉपर सल्फेट से प्राप्त कॉपर की मात्रा = [latex]\frac { 63.5 }{ 159.5 } \times 100[/latex]= 39.81 g .
प्रश्न 8.
आयरन के ऑक्साइड का आण्विक सूत्र ज्ञात कीजिए जिसमें आयरन तथा ऑक्सीजन का द्रव्यमान प्रतिशत क्रमशः 69.9 g तथा 30.1 g है।
हल
मूलानुपाती सूत्र की गणना के लिए प्रश्न 3 का हल देखिये।।
प्रश्न 9.
निम्नलिखित आँकड़ों के आधार पर क्लोरीन के औसत परमाणु द्रव्यमान का परिकलन कीजिए-
उत्तर
क्लोरीन का औसत परमाणु द्रव्यमान![]()
प्रश्न 10.
एथेन (C2H6) के तीन मोलों में निम्नलिखित का परिकलन कीजिए-
(i) कार्बन परमाणुओं के मोलों की संख्या
(ii) हाइड्रोजन परमाणुओं के मोलों की संख्या
(iii) एथेन के अणुओं की संख्या।
उत्तर
- 1 मोल एथेन में कार्बन परमाणुओं के 2 मोल हैं।
∴ 3 मोल एथेन में उपस्थित कार्बन परमाणुओं के मोलों की संख्या = 3×2=6 - 1 मोल एथेन में हाइड्रोजन परमाणुओं के 6 मोल हैं।
∴ 3 मोल एथेन में उपस्थित हाइड्रोजन परमाणुओं के मोलों की संख्या =3×6=18 - 1 मोल एथेन में उपस्थित अणु = 6.022×1023 (आवोगाद्रो संख्या)
∴ 3 मोल एथेन में उपस्थित अणुओं की संख्या = 3x 6.022x 1023 = 18.066×1023
प्रश्न 11.
यदि 20 g चीनी (C2H22O11) को जल की पर्याप्त मात्रा में घोलने पर उसका आयतन 2L हो जाए तो चीनी के इस विलयन की सान्द्रता क्या होगी?
उत्तर
चीनी का मोलर द्रव्यमान = (12×12)+ (1×22) + (11×16) = 342 g mol-1
Class 11th रसायन विज्ञान की कुछ मूल अवधारणाएँ Solution - RDS TEAM
प्रश्न 12.
यदि मेथेनॉल का घनत्व 0.793 kgL-1हो तो इसके 0.25 M के 2.5L विलयन को बनाने के लिए कितने आयतन की आवश्यकता होगी?
उत्तर
मेथेनॉल का मोलर द्रव्यमान (CH3OH)= 32 g mol-1
दिये गये विलयन को तैयार करने के लिए आवश्यक मेथेनॉल का भार, जो निम्नवत् है-
अतः आवश्यक मेथेनॉल प्रतिदर्श का आयतन = 25.22 mL
प्रश्न 13.
दाब को प्रति इकाई क्षेत्रफल पर लगने वाले बल के रूप में परिभाषित किया जाता है। दाब का S.I. मात्रक पास्कल नीचे दिया गया है-
1 Pa=1Nm-2
यदि समुद्रतल पर हवा का द्रव्यमान 1034 g cm-2हो तो पास्कल में दाब का परिकलन कीजिए।
उत्तर
दाब को प्रति इकाई क्षेत्रफल पर लगने वाले बल के रूप में परिभाषित किया गया है।
समुद्रतल पर हवा का भार = mXg = 1034×98 = 10.1332 kg ms-2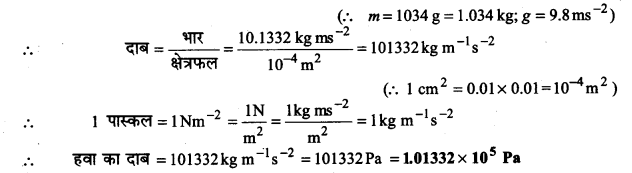
प्रश्न 14.
द्रव्यमान का S.I. मात्रक क्या है? इसे किस प्रकार परिभाषित किया जाता है?
उत्तर
द्रव्यमान का S.I. मात्रक किलोग्राम (kg) है। पेरिस के निकट सैवरेस में 0°C पर रखी प्लैटिनम-इरीडियम मिश्र-धातु की एक विशेष छड़ अथवा टुकड़े का द्रव्यमान 1 मानक किलोग्राम माना गया है।
Class 11th रसायन विज्ञान की कुछ मूल अवधारणाएँ Solution - RDS TEAM
प्रश्न 15.
निम्नलिखित पूर्व-लग्नों को उनके गुणांकों के साथ मिलाइए-
उत्तर
- माइक्रो-10-6,
- डेका-10,
- मेगा–10°,
- गीगा–10,
- फेम्टो-10-15
प्रश्न 16.
सार्थक अंकों से आप क्या समझते हैं?
उत्तर
उन अंकों की संख्या को, जिनके द्वारा किसी राशि को निश्चित रूप से व्यक्त किया जाता है. सार्थक अंक कहते हैं।
प्रश्न 17.
पेय जल के नमूने में क्लोरोफॉर्म, जो कैन्सरजन्य है, से अत्यधिक संदूषित पाया गया। संदूषण का स्तर 15 Ppm (द्रव्यमान के रूप में था।
(i) इसे द्रव्यमान प्रतिशतता में दर्शाइए।
(ii) जल के नमूने में क्लोरोफॉर्म की मोललता ज्ञात कीजिए।
उत्तर
(i) 15 ppm (द्रव्यमान द्वारा) का अर्थ है कि क्लोरोफॉर्म के 15 भाग (द्रव्यमान से) पानी के 106 भाग (द्रव्यमान से) में उपस्थित हैं।
प्रश्न 18.
निम्नलिखित को वैज्ञानिक संकेतन में लिखिए-
(i) 0.0048
(ii) 234.000
(iii) 8008
(iv) 500.0
(v) 6.0012
उत्तर
(i) 4.8×10-3,
(ii) 234×105,
(iii) 8.008×103,
(iv) 5.000×102,
(v) 60012×100
प्रश्न 19.
निम्नलिखित में सार्थक अंकों की संख्या बताइए-
(i) 0.0025
(ii) 208
(iii) 5005
(iv) 126,000
(v) 500.00
(vi) 2.0034
उत्तर
(i) 2,
(ii) 3,
(iii) 4,
(iv) 6,
(v) 3,
(vi) 5
प्रश्न 20.
निम्नलिखित को तीन सार्थक अंकों तक निकटित कीजिए-
(i) 34.216
(ii) 10.4107
(iii) 0.04597
(iv) 2808
उत्तर
(i) 34.2,
(ii) 10.4,
(iii) 0.0460,
(iv) 2810
प्रश्न 21.
(क) जब डाइनाइट्रोजन और डाइऑक्सीजन अभिक्रिया द्वारा भिन्न यौगिक बनाती हैं। तो निम्नलिखित आँकड़े प्राप्त होते हैं-
ये प्रायोगिक आँकड़े रासायनिक संयोजन के किस नियम के अनुरूप हैं? बताइए।
(ख) निम्नलिखित में रिक्त स्थान को भरिए-
उत्तर
(क) यदि नाइट्रोजन का द्रव्यमान 28 g स्थिर माना जाये तो इन चारों स्थितियों में ऑक्सीजन का द्रव्यमान क्रमशः 32 g, 64 g, 32 g और 80 g प्राप्त होता है, जो सरल पूर्ण संख्या अनुपात । 2 : 4 : 2 : 5 में हैं। अतः दिये गये आँकड़े गुणित अनुपात के नियम का पालन करते हैं।
Class 11th रसायन विज्ञान की कुछ मूल अवधारणाएँ Solution - RDS TEAM
प्रश्न 22.
यदि प्रकाश का वेग 3.00 x 108 ms-1 हो तो 2.00 ns में प्रकाश कितनी दूरी तय करेगा?
उत्तर
तय दूरी = वेग x समय = 30×108 ms-1x200 ns
= 3.0×108 ms-1x200nsx[latex]\frac { { 10 }^{ -9 }s }{ 1ns } [/latex]= 6.00×10-1m=0.600 m
प्रश्न 23.
किसी अभिक्रिया A+B2→AB, में निम्नलिखित अभिक्रिया मिश्रणों में सीमान्त अभिकर्मक, (यदि कोई हो तो) ज्ञात कीजिए-
(i) A के 300 परमाणु + B के 200 अणु
(ii) 2 मोल A+3 मोल B
(iii) A के 100 परमाणु + B के 100 अणु
(iv) A के 5 मोल + B के 2-5 मोल
(v) A के 25 मोल+ B के 5 मोल
उत्तर
- दी गई अभिक्रिया के अनुसार, A + B2 → AB2 A का एक परमाणु AB के एक अणु से अभिक्रिया करता है।
∴ पूर्ण अभिक्रिया में A के 300 परमाणुओं के लिए, B के 300 अणुओं की आवश्यकता होगी। क्योंकि B के केवल 200 अणु उपस्थित हैं, अतः 100 अणुओं की कमी है। इस प्रकार A अधिकता में है। इसलिए B एक सीमान्त अभिकर्मक है। - A के 1 मोल, B के 1 मोल से अभिक्रिया करते हैं।
∴ A के 2 मोल, B के 2 मोल से अभिक्रिया करेंगे B के 3 मोल उपस्थित हैं जो अधिकता में हैं। इस प्रकार A एक सीमान्त अभिकर्मक है। - A के 100 परमाणु B के 100 अणुओं से पूरी तरह अभिक्रिया करेंगे। इस प्रकार दोनों प्रयुक्त हो जायेंगे। अत: इस स्थिति में कोई सीमान्त अभिकर्मक नहीं होगा।
- B के 2.5 मोल, A के 2.5 मोल के साथ अभिक्रिया करेंगे। इस प्रकार A अधिकता में बचा रहेगा। अतः, B एक सीमान्त अभिकर्मक है।
- A के 2.5 मोल B के 2.5 मोल के साथ अभिक्रिया करेंगे। इस प्रकारे B अधिकता में बचा रहेगा। अतः A एक सीमान्त अभिकर्मक है।
प्रश्न 24.
डाइनाइट्रोजन और डाइहाइड्रोजन निम्नलिखित रासायनिक समीकरण के अनुसार अमोनिया बनाती हैं-
N2(g) + 3H2(g) → 2NH3(g)
(i) यदि 2-00×103g डाइनाइट्रोजन 1-00×103 g डाइहाइड्रोजन के साथ अभिक्रिया करती है तो प्राप्त अमोनिया के द्रव्यमान का परिकलन कीजिए।
(ii) क्या दोनों में से कोई अभिकर्मक शेष बचेगा?
(iii) यदि हाँ, तो कौन-सा उसका द्रव्यमान क्या होगा?
उत्तर
स्पष्ट है, डाइहाइड्रोजन अधिकता में है तथा डाइनाइट्रोजन एक सीमान्त अभिकर्मक है।
∵ 28 g डाइनाइट्रोजन से उत्पन्न अमोनिया = 34g![]()
(ii) डाइहाइड्रोजन शेष बचेगा।
(iii) शेष H, का द्रव्यमान = 1.00×10-3 – 428.57=571.43 g
Class 11th रसायन विज्ञान की कुछ मूल अवधारणाएँ Solution - RDS TEAM
प्रश्न 25.
0.5 मोल Na2CO3और 0.50 M Na2CO3 में क्या अन्तर है?
उत्तर
Na2CO3 का मोलर द्रव्यमान = (2×23) +12+ (3×16)= 106
0.5 मोल Na2CO3 से तात्पर्य है-
05×106= 53g Na2CO3
यह केवल द्रव्यमान को सन्दर्भित करता है।
0.50 M Na2CO3 से तात्पर्य है 0.50 मोलर, अर्थात् Na2CO3 के 53 gm 1 लीटर विलयन में उपस्थित हैं। इस प्रकार यह विलयन के सान्द्रण को बताता है।
प्रश्न 26.
यदि डाइहाइड्रोजन गैस के 10 आयतन डाइऑक्सीजन गैस के 5 आयतनों के साथ अभिक्रिया करें तो जलवाष्प के कितने आयतन प्राप्त होंगे?
उत्तर![]()
हाइड्रोजन (H2) के दो आयतन ऑक्सीजन (O2) के एक आयतन के साथ अभिक्रिया करके जल वाष्प (H20) के दो आयतन उत्पन्न करते हैं।
इस प्रकार H2 के 10 आयतन पूर्णत: O2, के 5 आयतन के साथ अभिक्रिया करके जलवाष्प के 10 आयतन उत्पन्न करेंगे।
प्रश्न 27.
निम्नलिखित को मूल मात्रकों में परिवर्तित कीजिए-
(i) 28.7 pm
(ii) 15.15 us
(iii) 25365 mg
उत्तर
प्रश्न 28.
निम्नलिखित में से किसमें परमाणुओं की संख्या सबसे अधिक होगी?
(i) 1g Au(s)
(ii) 1 g Na(s)
(iii) 1g Li(s)
(iv) 1 g Cl2(g)
उत्तर
इस प्रकार एक ग्राम लीथियम में परमाणुओं की संख्या सबसे अधिक है।
प्रश्न 29.
एथेनॉल के ऐसे जलीय विलयन की मोलरता ज्ञात कीजिए जिसमें एथेनॉल का मोल-अंश 0.040 है।
उत्तर
इस प्रकार एक लीटर विलयन में एथेनॉल के 2.314 मोल उपस्थित हैं। अत: दिये गये विलयन की मोलरता = 2.314 M
प्रश्न 30.
एक 12c कार्बन परमाणु का ग्राम (g) में द्रव्यमान क्या होगा?
उत्तर
12c के एक मोल अर्थात् 6.022×1023 परमाणुओं का द्रव्यमान 12g होता है।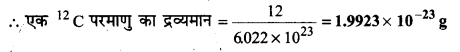
प्रश्न 31.
निम्नलिखित परिकलनों के उत्तर में कितने सार्थक अंक होने चाहिए?
(i) [latex]\frac { 0.02856\times 298.15\times 0.112 }{ 0.5785 } [/latex]
(ii) 5×5.364
(iii) 0.0125 + 0.7864 + 0.0215
उत्तर
(i) न्यूनतम यथार्थ परक संख्या (0.112) में तीन सार्थक अंक हैं। अत: उत्तर में तीन सार्थक अंक होने चाहिए।
(ii) पाँच पूर्ण संख्या हैं। दूसरी संख्या अर्थात् 5.364 में 4 सार्थक अंक है। अत: उत्तर में चार सार्थक अंक होने चाहिए।
(iii) उत्तर में चार सार्थक अंक होने चाहिए क्योंकि दशमलव स्थानों की न्यूनतम संख्या 4 है।
प्रश्न 32.
प्रकृति में उपलब्ध ऑर्गन के मोलर द्रव्यमान की गणना के लिए निम्नलिखित तालिका में-
उत्तर
ऑर्गन का औसत मोलर द्रव्यमान
प्रश्न 33.
निम्नलिखित में से प्रत्येक में परमाणुओं की संख्या ज्ञात कीजिए-
(i) 52 मोल Ar
(ii) 52u He
(iii) 52 g He
उत्तर
(i) ऑर्गन का 1 मोल = 6.022×1023परमाणु
∴ ऑर्गन के 52 मोल = 52x 6.022×1023 परमाणु = 3.131×1025 परमाणु
(ii) He के 4u = He का एक परमाणु
∴ He के 52u = [latex]\frac { 52 }{ 4 } [/latex] = 13 परमाणु
(iii) He के एक मोल अर्थात् इसके 4 g में 6.022×103 परमाणु उपस्थित होते हैं।
अतः 52 g He में उपस्थित परमाणुओं की संख्या = [latex]\frac { 6.022\times { 10 }^{ 23 } }{ 4 } \times 52[/latex]
= 3.131×1025 परमाणु
प्रश्न 34.
एक वेल्डिंग ईंधन गैस में केवल कार्बन और हाइड्रोजन उपस्थित हैं। इसके नमूने की कुछ मात्रा ऑक्सीजन से जलाने पर 3.38 g कार्बन डाइऑक्साइड, 0.690 g जल के अतिरिक्त और कोई उत्पाद नहीं बनाती। इस गैस के 10.0L (STP पर मापित) आयतन का द्रव्यमान 11.69 g पाया गया। इसके-
(i) मूलानुपाती सूत्र
(ii) अणु द्रव्यमान और
(iii) अणुसूत्र की गणना कीजिए।
उत्तर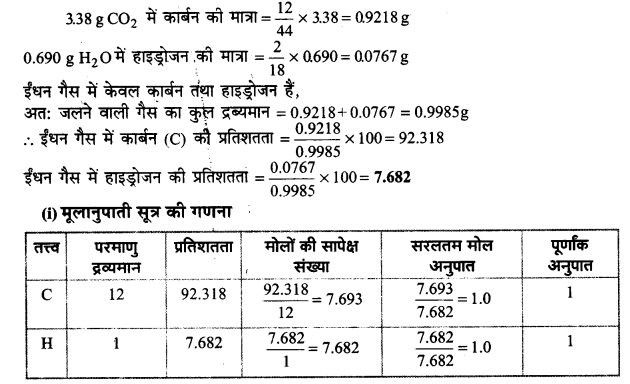

प्रश्न 35.
CaCO3 जलीय HCI के साथ निम्नलिखित अभिक्रिया कर CaCI2 और C02 बनाता है।
CaC03(s) + 2HCI(g) → CaCl2(aq) + C02(g) + H2O(l) 0.75 M-HCI के 25 mL के साथ पूर्णतः अभिक्रिया करने के लिए CaCO3 की कितनी मात्रा की आवश्यकता होगी?
उत्तर
विलयन की मोलरता (M) निम्न सम्बन्ध से प्राप्त की जा सकती है-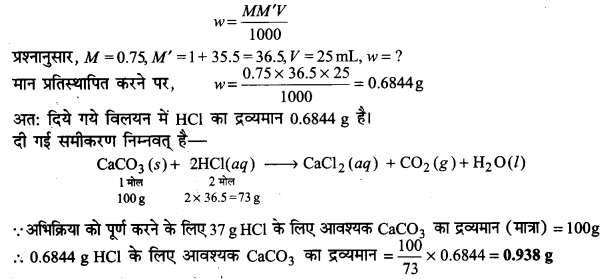
प्रश्न 36.
प्रयोगशाला में क्लोरीन का विरचन मैंगनीज डाइऑक्साइड (MnO2) की जलीय HCI विलयन के साथ अभिक्रिया द्वारा निम्नलिखित समीकरण के अनुसार किया जाता है| 4HCI(aq) + MnO2(s) → 2H20(l) + MnCl2(aq) + Cl2(g)
5.0 g मैंगनीज डाइऑक्साइड के साथ HCI के कितने ग्राम अभिक्रिया करेंगे?
उत्तर
दी गई समीकरण निम्नवत् है-
Class 11th रसायन विज्ञान की कुछ मूल अवधारणाएँ Solution - RDS TEAM








0 Comments